Experten weltweit warnen: Die Ausbreitung antibiotikaresistenter Bakterien stellt eine der größten Gefahren für die Gesellschaft dar – größer als Terrorismus oder Klimawandel.
In Europa und den USA sterben jährlich mindestens 50.000 Menschen an Infektionen, die auf herkömmliche Antibiotika nicht ansprechen. Diese "Antibiotika-Apokalypse" ist bereits im Gange.
Was ist Antibiotikaresistenz?
Seit der Entdeckung von Penicillin 1928 haben Bakterien Strategien entwickelt, um Antibiotika zu widerstehen. Sie werden nicht getötet, und ihr Wachstum wird nicht gestoppt. Solche resistenten Stämme gibt es weltweit. Bei anhaltenden Trends könnten Antibiotika in wenigen Jahrzehnten nutzlos werden.
Laut dem Bericht des Review on Antimicrobial Resistance könnte bis 2050 die Weltbevölkerung um fast eine halbe Milliarde schrumpfen und die Weltwirtschaft 100 Billionen Dollar kosten.
Mehr zu Antibiotikaresistenz:
- Die neun gefährlichsten antibiotikaresistenten Bakterien
- Ist Antibiotikaresistenz wirklich so schlimm wie der Klimawandel?
Warum sind Antibiotika so wichtig?
Antibiotika töten Bakterien oder hemmen ihr Wachstum und behandeln Infektionen von leichten Hauterkrankungen wie Akne bis zu schweren Erkrankungen wie Lungenentzündung, Tuberkulose oder Meningitis.
Sie schützen Wunden nach Verletzungen oder Operationen und unterstützen Patienten mit geschwächtem Immunsystem, etwa bei Krebs oder nach Organtransplantationen. Es gibt Hunderte Varianten – von Cremes bis Injektionen. Seit ihrer Einführung vor rund 75 Jahren haben sie die globale Lebenserwartung um etwa 20 Jahre verlängert.
Vor Antibiotika waren Infektionen oft tödlich: Etwa 40 Prozent aller Todesfälle resultierten aus unbehandelten Infektionen, die Narben oder Verunstaltungen hinterließen.
Mehr zu Bakterien:
- Das Experiment, das bewies, dass Bakterien Krankheiten verursachen
- Bin ich mehr Bakterien als Mensch?
Wie wirken Antibiotika?
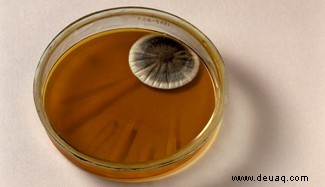
Antibiotika stören zentrale Prozesse in Bakterienzellen, ohne menschliches Gewebe zu schädigen. Penicillin, entdeckt von Alexander Fleming, lässt Bakterienzellwände kollabieren – menschliche Zellen haben keine solchen Wände.
Andere Antibiotika blockieren Protein-, DNA- oder Energieproduktion in Bakterien.

Wie werden Bakterien resistent?
Resistenz ist ein natürlicher Evolutionsprozess. Bei der Vermehrung entstehen Mutationen in der DNA. In Milliarden von Zellen entwickeln einige Varianten Immunität, z. B. durch veränderte Zielmoleküle oder Enzyme wie Beta-Lactamasen, die Penicillin neutralisieren.
Resistenzgene werden via horizontalem Gentransfer zwischen Bakterien geteilt – von harmlosen zu pathogenen Stämmen.
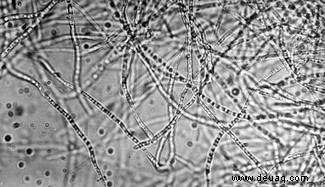
Resistenzen betreffen nicht nur Bakterien, sondern auch Viren, Pilze und Parasiten (AMR). Selbst Insekten und Unkräuter widerstehen Pestiziden.
Wie breitet sich Resistenz aus?
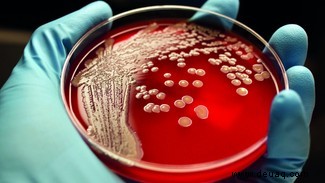
Übermäßiger Antibiotikaeinsatz tötet sensible Bakterien, lässt Resistente dominieren. Betroffene übertragen sie weiter. Krankenhäuser sind Hotspots durch hohen Einsatz.
In der Tierhaltung fördern Wachstumshemmer und Präventivgaben das Problem. Globale Reisen verbreiten Resistenzen rasch.
Was, wenn Antibiotika versagen?
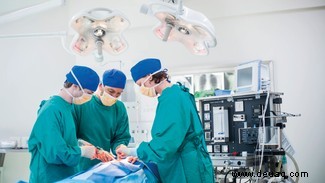
Todesfälle durch Infektionen wie Tuberkulose oder Meningitis würden explodieren. Routineeingriffe wie Kaiserschnitte oder Operationen wären riskant. Gesundheitssysteme könnten kollabieren.
Mehr zur Zukunft von Bakterien:
- Die Bakterien lösen ein sensibles Problem
- Wundermikroben: Sieben Bakterien, die unsere Zukunft antreiben
Wie besorgt sollten wir sein?
Sehr! Multiresistente "Superbugs" wie MRSA oder XDR-TB belasten Systeme. Prof. Dame Sally Davies, Ex-Chief Medical Officer UK, fürchtet Routineoperationen mehr als Klimawandel.
XDR-TB tötet jährlich über 200.000 Menschen in 100 Ländern. Bei E. coli scheitert Standardtherapie bei über 50 Prozent. Letzte-Linie-Antibiotika versagen bereits.

Können wir nicht neue Antibiotika entwickeln?
Früher ja, doch seit den 1990ern fehlen innovative Ansätze. Kosten: 500 Mio. bis 2 Mrd. Dollar pro Medikament. Resistenzen machen sie schnell unwirksam – wenig Anreiz für Pharma.
Positive News: 2017 modifizierte das Scripps Research Institute Vancomycin für dreifachen Angriff, resistentearm.

Gibt es Alternativen?
Kombitherapien blockieren Resistenzmechanismen. Phagentherapie (seit 1940er in Osteuropa) nutzt Viren gegen Bakterien. Weitere: Immunboosts, Nanopartikel, Probiotika.
- Warum Sie BBC Science Focus abonnieren sollten

Was können wir tun?
Globale Koordination: Nur bei bakteriellen Infektionen verschreiben, richtige Dosis/Dauer. Schnelle Tests, Hygiene, kein Druck auf Ärzte.
Mehr zu Hygiene:
- Körperpflege: Gibt es "zu sauber"?
- Warum hat Salz antibakterielle Eigenschaften?
Schätzen wir Antibiotika – je sparsamer, desto länger wirksam.