Wissenschaftler sind ein vorsichtiger Haufen, der gerne einen Vorbehalt macht, selbst wenn er seine eigene Forschung beschreibt. „Unsere Lieblingsausdrücke sind ‚Ja, aber…‘ und ‚Andererseits…‘ und ‚Es bleibt unklar…‘“, sagt Gene Editor Dr. Fyodor Urnov. „Also bitte fügen Sie all das zu dem hinzu, was ich gleich sagen werde.
„Wenn CRISPR 10 Prozent dessen verwirklicht, wovon wir Praktiker der Genbearbeitung träumen, wird es mit den größten Fortschritten in der Geschichte der Biomedizin als Technologie mit Auswirkungen auf die öffentliche Gesundheit konkurrieren.“
Urnov spricht über einen knackigen Zoom-Link aus seinem Büro am Innovative Genomics Institute (IGI) in Berkeley, Kalifornien, das an der Spitze dessen steht, was sich als der entscheidende wissenschaftliche Durchbruch des 21. Jahrhunderts erweisen könnte.
CRISPR ist eine Genom-Editierungstechnologie, die es Wissenschaftlern ermöglicht, DNA mit unglaublicher Präzision zu schneiden und DNA einzufügen oder zu löschen, um unerwünschte Mutationen zu korrigieren. Um die Technologie zu stark zu vereinfachen, es ist die Fähigkeit, die Bausteine des Lebens zu bearbeiten, genau wie Text auf einem Computerbildschirm. Es könnte Wissenschaftlern nicht nur ermöglichen, Gene auszuschalten, die zu einem breiten Spektrum von Krankheiten führen, sondern es wird uns alle von der Genetik befreien, mit der wir geboren wurden.
„Die gewonnenen Erkenntnisse sind erstaunlich und es ist einfach eine wirklich beschleunigte Grundlagenforschung. Das allein ist schon transformierend“, sagt Dr. Robin Lovell-Badge vom Crick Institute. „Und die Vorstellung, dass wir Menschen mit genetischen Krankheiten tatsächlich auf eine Weise behandeln können, die vorher nie möglich war, ist umwerfend.“
In den letzten zehn Jahren war die Technologie größtenteils auf das Labor beschränkt. Jetzt jedoch verändern die ersten CRISPR-Therapien das Schicksal von Menschen, die mit schwächenden Erbkrankheiten geboren wurden. Die meisten von uns haben es noch nicht erkannt, aber wir befinden uns am Fuße einer tiefgreifenden medizinischen und technologischen Revolution, die nicht nur die Aussicht auf neue Behandlungen und Heilmittel aufwirft, sondern auch große Fragen zu Ethik, Gleichberechtigung und Gerechtigkeit im Gesundheitswesen. P>
Die ankommende Welle von Gen-Editing-Anwendungen wurde mit der Industriellen Revolution oder der Geburt des Internets in Bezug auf die bahnbrechenden Auswirkungen verglichen, die es auf die Gesellschaft haben wird.

Die Biochemikerin Dr. Jennifer Doudna gründete das IGI, um all dies und mehr anzugehen. Als Non-Profit-Organisation existiert das Institut nicht nur, um die Geneditierung zu erforschen, sondern sie auch erschwinglich und für jedermann zugänglich zu machen. Angesichts der Breite des CRISPR-Potenzials ist dies ein großer Anspruch, daher stimmte das Führungsteam des IGI zu, BBC Science Focus zu geben einen exklusiven Überblick über seine Bemühungen.
Dort auf dem Campus von Berkeley haben Doudna und Dr. Emmanuelle Charpentier vor fast einem Jahrzehnt die Welt verändert. Ihre Zusammenarbeit führte zur Entwicklung von CRISPR-Cas9, dem Gen-Editing-Tool, das 2012 in einer wegweisenden Arbeit beschrieben wurde, die mit dem Nobelpreis ausgezeichnet wurde.
„Ich glaube, wir hatten beide ein bisschen das Gefühl von, weißt du, einer Art Erkältung“, sagt sie. „Ich erinnere mich noch an dieses Gefühl von Nackenhaaren, wenn ich dachte, dass hier etwas wirklich Interessantes ist. Und ich würde wetten, dass keiner von uns damals eine Ahnung hatte, wo es enden würde, denn ich glaube nicht, dass man das jemals tut.“
CRISPR ist nicht die einzige Gen-Editing-Technologie und das IGI ist nicht das einzige Institut, das auf diesem Gebiet Pionierarbeit leistet. Aber CRISPR ist vielseitiger, benutzerfreundlicher und billiger als viele andere Technologien. Und was erstaunlich ist, ist die Geschwindigkeit des Fortschritts. In weniger als einem Jahrzehnt ist es von der Entdeckung zu Versuchen am Menschen und potenziellen Heilmitteln übergegangen, etwas, das in der Biomedizin praktisch unbekannt ist.
„Es ist ein bisschen wie ein Schleudertrauma“, sagt Dr. Brad Ringeisen, Geschäftsführer des IGI. „Denken Sie an Nanopartikel, die Nano-Revolution. Pfizer hat Nanopartikel in seinem COVID-mRNA-Impfstoff, aber diese [Technologie] hat 30 oder 40 Jahre gedauert.“
Die ersten Erfolge von CRISPR
Menschen, die mit Sichelzellenanämie geboren wurden, werden zu den ersten gehören, die von Fortschritten in der Genbearbeitung profitieren werden. Im Jahr 2019 wurde eine Frau namens Victoria Gray als eine der ersten Menschen weltweit wegen einer genetisch vererbten Krankheit mit einer CRISPR-basierten Therapie behandelt.
Sie wurde mit Sichelzellenanämie geboren und benötigte starke Schmerzmittel und regelmäßige Bluttransfusionen, um die Auswirkungen des mutierten Gens abzuwehren, das die roten Blutkörperchen krümmt und den Blut- und Sauerstofffluss im Körper blockiert. Abgesehen von quälenden Schmerzanfällen kann Sichelzellenanämie zu Schlaganfall, Bluthochdruck, Organschäden und mehr führen.
Die Behandlung war nicht einfach. Die Ärzte entfernten Gray und den anderen Patienten in der Studie Knochenmarkszellen und benutzten dann CRISPR, um ein Gen zu bearbeiten, das die Produktion von fötalem Hämoglobin aktiviert, einem Protein, das die Symptome der Sichelzellenanämie lindern kann. Die Patienten wurden dann einer Chemotherapie unterzogen, um den größten Teil ihres Knochenmarks zu zerstören, woraufhin Milliarden bearbeiteter Zellen wieder in ihren Körper infundiert wurden.

Gray benötigt keine Medikamente oder Transfusionen mehr, ebenso wenig wie die anderen Personen in ihrer Studie, zu der auch Patienten mit einer verwandten Bluterkrankung gehörten. Es scheint, dass eine einmalige CRISPR-Behandlung sie geheilt hat.
„Die Sichelzellkrankheit ist wahrscheinlich das einfachste Ziel, das die meisten Menschen betrifft“, sagt Ringeisen. „Es ist so einfach wie möglich:Sie gehen hinein und schalten entweder ein alternatives Gen ein oder Sie versuchen, das eine zu korrigieren. Einhunderttausend Menschen in den Vereinigten Staaten haben Sichelzellenanämie und ich denke, es sind über eine Million Menschen weltweit. Es gibt also einen enormen Einfluss, der erzielt werden kann.“
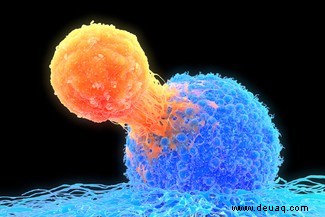
Das IGI bereitet einen eigenen Sichelzellenversuch vor, aber der Aufgabenbereich des Instituts umfasst auch viele andere Bedingungen. Neben Blutkrankheiten betreibt es aktive Forschungsprojekte zu Autoimmunerkrankungen, neurologischen Erkrankungen, Krebs und COVID-19. Ein vielversprechender Forschungsweg sind T-Zellen, die manchmal als Truppen vor Ort unseres Immunsystems bezeichnet werden.
Dr. Alex Marson, Direktor für menschliche Gesundheit des IGI, betreibt ein Labor, das daran arbeitet, T-Zellen mit CRISPR zur Behandlung verschiedener Arten von Krankheiten zu entwickeln. Er plant derzeit eine klinische Studie mit einer Familie, in der eine starke genetische Mutation verschiedene Manifestationen von Autoimmunerkrankungen in der jüngeren Generation verursacht hat.
„Im Labor haben wir Zellen dieser Kinder korrigiert“, sagt er. „Jetzt arbeiten wir an einer klinischen Studie, um diese genkorrigierten T-Zellen zu nehmen und sie mindestens einem dieser jungen Erwachsenen zu infundieren, um zu versuchen, das Gleichgewicht im System wiederherzustellen und die Autoimmunkrankheit zu behandeln.“
Während aktuelle T-Zelltherapien sehr teuer sind, stellt sich Marson eine Zukunft vor, in der T-Zellen von der Stange hergestellt werden, um verschiedene Arten von Krankheiten zu behandeln, und ihre Produktion in einem Umfang industrialisiert wird, der sie für jeden zugänglich macht, der sie benötigt. P> 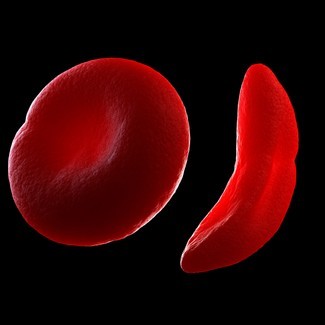
„Wir können Infektionskrankheiten behandeln, indem wir Immunzellen entwickeln, die Infektionen erkennen“, sagt er. „Ich denke, wir werden diese Art von flexibler Fähigkeit haben, die Sprache der DNA tatsächlich in die Immunzelle zu schreiben und sie in einer Arzneimittelplattform zu verwenden.“
Hier wird es erst richtig interessant, denn es zeigt, wie breit die medizinischen Anwendungen von CRISPR sein werden. Sein Potenzial liegt nicht nur in den Zuständen, die durch eine einzelne genetische Mutation wie die Sichelzellkrankheit verursacht werden, sondern in jeder Krankheit, die eine genetische Komponente hat, entweder in Bezug auf Anfälligkeit oder Schutz.
Dazu gehören viele der Haupttodesursachen, darunter Krebs, Herz-Kreislauf-Erkrankungen und neurodegenerative Erkrankungen sowie chronische Erkrankungen wie entzündliche Darmerkrankungen und rheumatoide Arthritis.
„Alle Krankheiten sind auf der Karte“, sagt Ringeisen.
Vorbeugung von Krankheiten
Ein Teil dessen, was Wissenschaftler optimistisch stimmt, ist, dass Gen-Editierung verwendet werden kann, um einer Person schützende DNA zu verleihen und unerwünschte Mutationen zu korrigieren.
„Wir wissen, dass Sie eine genetische Veränderung vornehmen können, die Ihr Risiko für Herzerkrankungen drastisch senkt“, sagt Urnov. „Woher wissen wir das? Wegen sehr seltener Individuen, die diese genetischen Veränderungen haben. Und wenn Sie viele von ihnen studieren, ist es irgendwie umwerfend. Ich werde nicht sagen, dass sie immun gegen Herzkrankheiten sind, aber sie stehen kurz davor.“
Doudna glaubt, dass CRISPR sogar eher zur Vorbeugung als zur Behandlung von Krankheiten eingesetzt werden könnte. „Stellen Sie sich eine Zeit vor, in der Menschen ihr Genom sequenzieren lassen und erfahren, dass Sie ein Gen haben, das die Wahrscheinlichkeit erhöht, an Herz-Kreislauf-Erkrankungen zu erkranken“, sagt sie. „Aber Sie haben die Möglichkeit, Ihre Zellen zu bearbeiten, damit Sie nicht warten müssen, um herauszufinden, ob Sie zu den Pechvögeln gehören, die anfällig sind.“
Heutzutage ergreifen viele von uns vorbeugende Maßnahmen, um unsere zukünftige Gesundheit zu schützen. Es könnte alles sein, von einer ballaststoffreichen Ernährung, um Herzkrankheiten in Schach zu halten, bis hin zu einer doppelten Mastektomie, weil Brustkrebs in der Familie liegt. Würden Sie gerne Ihre DNA bearbeiten, um die gleichen Ergebnisse zu erzielen?
Es ist schwieriger, die Kosten-Nutzen-Analyse durchzuführen, wenn Sie über solche experimentellen Therapien sprechen. Einige werden sagen, dass jede Form der Genbearbeitung „Gott spielt“, und Verschwörungstheorien rund um COVID-19-Impfstoffe zeigen, wie sich Misstrauen gegenüber neuen Technologien ausbreiten kann.
„Es können falsche Darstellungen oder einfach nur Missverständnisse in der öffentlichen Denkweise verankert sein, die sich negativ auf das auswirken können, was meiner Meinung nach positive Fortschritte sein sollte“, sagt Doudna. „Ein weiteres Beispiel dafür ist die gesamte Anti-GMO-Bewegung.“
Im November 2018 wurden in China Zwillingsmädchen geboren, die sogenannten CRISPR-Babys. Der Biophysiker Dr. He Jiankui gab bekannt, dass er die weltweit ersten genomeditierten Babys geschaffen hatte, was zu weit verbreiteter Verurteilung führte.

Er konstruierte Mutationen in menschlichen Embryonen, die später einer Frau implantiert wurden, und überschritt eine ethische Grenze, indem er die menschliche Keimbahn veränderte, was bedeutete, dass die von ihm vorgenommenen Änderungen auch an zukünftige Generationen weitergegeben würden. Außerdem wurde er dafür kritisiert, dass er die normalen Sicherheitsverfahren missachtete.
Jiankui behauptete, er habe ein Gen namens CCR5 deaktiviert, das Schutz vor HIV biete. Seine Kritiker wiesen darauf hin, dass er auch versehentlich Mutationen in anderen Teilen des Genoms verursacht haben könnte. Jiankui wurde Anfang 2020 in China für drei Jahre inhaftiert und zur Zahlung einer Geldstrafe von drei Millionen Yuan (ca. 240.000 £) verurteilt
„Dieses Feld ist experimentell und wir sind ein ‚schwerwiegendes unerwünschtes Ereignis‘ der gesamten Bemühungen, die eingefroren werden“, sagt Urnov. „Das Schmerzliche für mich und für Zehntausende von Menschen wie mich, die 40 Jahre damit verbracht haben, menschliche Gentechnik zur Behandlung von Krankheiten zu entwickeln, wissen Sie, dass diese Technologie jetzt mit dem Konzept von Designer-Babys befleckt ist.
„Wir haben 250 Millionen Menschen auf dem Planeten Erde mit genetisch bedingten Krankheiten. Wir sollten nicht davon sprechen, irgendjemanden zu entwerfen. Wir sollten unsere ganze Aufmerksamkeit auf die Tatsache richten, dass es Hunderte von Millionen unserer Mitmenschen gibt, denen ihr Schicksal auf dem genetischen Teller überreicht wurde“, fügt er hinzu.
Auch andere Herausforderungen gilt es zu meistern. Einer der Hauptkritikpunkte an Jiankuis Arbeit ergibt sich aus der Tatsache, dass die Genbearbeitung noch nicht so präzise ist, dass Wissenschaftler absolut davon überzeugt sind, dass jede Bearbeitung nur den Teil des Genoms betrifft, auf den sie abzielt. Es kann zu sogenannten „Off-Target“-Effekten kommen:unbeabsichtigte genetische Veränderung, die an anderer Stelle des Zielgenoms auftritt. Ein Worst-Case-Szenario in klinischer Hinsicht könnte „Genotoxizität“ sein, bei der ein Off-Target-Effekt DNA-Schäden verursacht, die zu Krebs führen können.
Aus diesem Grund ist die sogenannte „Delivery Challenge“ von CRISPR ein wichtiger Forschungsschwerpunkt, sowohl am IGI als auch darüber hinaus.

„Wir können nur Vertrauen in die Sicherheit dieser Verfahren gewinnen, indem wir klinische Studien durchführen“, sagt Dr. Ross Wilson, Direktor für therapeutische Bereitstellung am IGI. „Wir sind nicht so anmaßend zu glauben, dass wir in der Lage sind, jedes mögliche Ergebnis vorherzusagen, wenn ein neues therapeutisches Verfahren versucht wird, weshalb diese Versuche methodisch und ohne Eile durchgeführt werden.“
„Sobald wir davon überzeugt sind, dass das Leben von Menschen gerettet oder zum Besseren verändert wird, ohne dass es zu unerwünschten Folgen kommt, kann die Technologie auf andere Anwendungen übertragen werden, um beispielsweise das Risiko von Herzerkrankungen zu verringern.“
Es gibt Möglichkeiten, dieses Risiko unbeabsichtigter Folgen der Genbearbeitung auszugleichen. Die eigenen Zellen eines Patienten können zur „Versuchsbearbeitung“ an das Labor gesendet werden, um einen fundierten Einblick in das zu erhalten, was wahrscheinlich im Körper des Patienten passiert, wenn sie dosiert werden.
Die CRISPRoff-Technologie befindet sich ebenfalls in der Entwicklung. Dieses Werkzeug ermöglicht es den Forschern, auf das Epigenom statt auf das Genom selbst abzuzielen. Das heißt, Wissenschaftler können ein bestimmtes Gen ausschalten, ohne einen DNA-Strang zu schneiden, indem sie stattdessen auf die Proteine und andere Moleküle abzielen, die sich an die DNA anheften und steuern, wann dieses Gen ein- oder ausgeschaltet wird. Da das Genom selbst unberührt ist, erwarten die Forscher ein geringeres Risiko unerwünschter Wirkungen.
„Die Pandemie hat uns gelehrt, dass die Öffentlichkeit ein großes Verlangen danach hat, Dinge als ‚sicher‘ oder ‚unsicher‘ zu erklären, aber in Wirklichkeit geht es nur um das Gleichgewicht zwischen Risiko und Nutzen“, sagt Wilson. „Dieses Verhältnis sieht für die CRISPR-Technologie äußerst vielversprechend aus und wird jedes Jahr besser, sodass die Zukunft für die therapeutische Genombearbeitung rosig ist.“
Könnte CRISPR eine gesundheitliche Ungleichheit schaffen?
Doudnas Traum für CRISPR ist es, es zum „Standard der medizinischen Versorgung“ zu machen. Dazu muss eine weitere Sache angegangen werden, die wohl komplexer ist als jede technische Hürde:die Behandlungskosten.
Die Genbearbeitung ist oder könnte ein großer Gleichmacher im Gesundheitswesen sein. Aber wie alle experimentellen Behandlungen ist es forschungsintensiv, arbeitsintensiv und teuer. Eine von Doudnas Befürchtungen ist, dass es zu einer Boutique-Technologie wird, die nur denen zur Verfügung steht, die es sich leisten können. Dies, sagt sie, würde nicht nur die bereits bestehende gesundheitliche Kluft zwischen Arm und Reich verschärfen, sondern auch eine neue Art von gesundheitlicher Ungleichheit schaffen:eine genetische Kluft.
Das IGI ist gemeinnützig und wird öffentlich und über Philanthropie finanziert. Seine Mitarbeiter sprechen nicht nur in technologischer, sondern auch in gesellschaftlicher Hinsicht über ihre Arbeit und konzentrieren sich darauf, wie die Reichweite der Technologie maximiert werden kann.
„Das ist ein großes Problem“, sagt Urnov. „In den USA werden einige dieser Medikamente für 2 Millionen Dollar verkauft, aber die europäischen Länder haben sich geweigert, sie überhaupt zu lizenzieren. Sie haben eine surreale Situation, in der Eltern in Europa, deren Kinder diese schweren Krankheiten haben, GoFundMe-Kampagnen starten, um amerikanische Preise zahlen zu können.
„Wir haben diese Lücke zwischen der Tatsache, dass diese Technologie in ihrem Nutzen schnell zunimmt, und wir kämpfen offen gesagt damit, wie wir sie gerecht und erschwinglich machen können.“
Hinzu kommt die Frage der Gesundheitsgerechtigkeit, die Tatsache, dass, wenn Sie mit einer Erbkrankheit geboren wurden, eine erschwingliche Heilung möglich sein kann, wenn genügend Menschen dieselbe Krankheit haben. Das würde es für Pharmaunternehmen wirtschaftlich tragfähig machen, in die Forschung zu investieren, um neue Behandlungen zu entwickeln.
Wenn Sie mit einer seltenen genetischen Mutation geboren werden, ist dies möglicherweise nicht möglich. „Es gibt diese schreckliche Lücke zwischen unserer Fähigkeit, die DNA dieser Person zu lesen und zu sagen:‚Ja, das ist die Mutation, die Ihre Mutter getötet hat und Sie töten wird, es tut mir leid, das zu sagen‘, und der tatsächlichen Entwicklung einer Behandlung, die dem helfen würde Person. Die Entwicklung solcher personalisierter Heilmittel hat im Wesentlichen keinen kommerziellen Wert. Niemand wird jemals Geld verdienen“, sagt Urnov.
Lovell-Badge stimmt zu. „Die Kosten sind ein Problem dafür, dass es für die öffentliche Gesundheit wirklich nützlich wird“, sagt er. „[Wir müssen] ganz am Anfang denken:‚Wie können wir das auf eine Weise machen, die erschwinglicher wird?‘ Dann geht man das Problem auf andere Weise an.“
Anders als so viele in der Biotech-Branche ist die Behandlung dieses Problems ein Eckpfeiler, auf dem das IGI aufgebaut wurde – nicht nur die Entwicklung neuartiger Behandlungen, sondern die Schaffung skalierbarer Pipelines für die Entdeckung, Erprobung und Einführung.
„Unsere Mission muss es wirklich sein, sicherzustellen, dass die Technologie allen zugute kommt“, sagt Doudna. „Das war überhaupt der Anstoß für das Innovative Genomics Institute. Viele Institute, viele Unternehmen, viele akademische Labore entwickeln jetzt Gen-Editing, aber nicht mit Blick auf die Kostenkontrolle und die wissenschaftliche Arbeit mit einem Fokus auf den öffentlichen Zugang zu dieser Technologie. Das ist wirklich unser Ziel.“
Die genetische Revolution kommt. Nachdem Doudna Pionierarbeit in der Technologie geleistet hat, besteht sie darauf, dass sie nach ihrer Ankunft für alle verfügbar ist. Wie mehr als einer ihrer Kollegen uns sagt, liegt das einfach in ihrer DNA.
- Dieser Artikel erschien zuerst in Ausgabe 367 des BBC Science Focus Magazine –